
Conteúdo extraído por Silvia Maria Ribeiro Oyama do livro Hospital and healthcare security, publicado em 2015 por Butterworth-Heinemann.
Ensaios Clínicos
Nas últimas aulas aprofundamos o conhecimento da Medicina Baseada em Evidências, e nesta aula vamos estudar as pesquisas denominadas de “ensaio clínico”. Os ensaios clínicos são pesquisas recomendadas para a tomada de decisão na prática assistencial.
Um ensaio clínico é um experimento controlado realizado em voluntários humanos. O objetivo desse tipo de pesquisa é avaliar a segurança e a eficácia de tratamentos ou intervenções contra as doenças e problemas de saúde de qualquer natureza, determinando os efeitos farmacológicos, farmacocinéticos e farmacodinâmicos de novas terapias, incluindo o estudo de reações adversas desses produtos.
Os ensaios clínicos são considerados estudos de excelência pois o pesquisador consegue controlar o máximo de variáveis e assim assegurar a validade do estudo.
O objeto de estudo pode ser intervenção terapêutica ou intervenção preventiva. É necessário haver dúvida suficiente sobre a eficácia de um tratamento, pois esse será oferecido para metade do grupo, e uma grande expectativa de que a intervenção seja benéfica, de forma a justificar a oferta à outra metade dos indivíduos.
As principais vantagens desse tipo de estudo incluem:
Os estudos de ensaio clínico são divididos em fases com objetivos específicos para cada etapa. As intervenções terapêuticas ou preventivas, após aprovação em todas as etapas, são autorizadas pelo órgão competente. No Brasil, a Agência Nacional de Vigilância Sanitária (ANVISA) é o órgão responsável pelo registro do novo medicamento que pode ser prescrito por médicos e dentistas.
Você conhece a ANVISA? A ANVISA tem como objetivo “promover a proteção da saúde da população, por intermédio do controle sanitário da produção e consumo de produtos e serviços submetidos à vigilância sanitária, inclusive dos ambientes, dos processos, dos insumos e das tecnologias a eles relacionados, bem como o controle de portos, aeroportos, fronteiras e recintos alfandegados” (ANVISA).
Saiba mais acessando o link: <http://portal.anvisa.gov.br/>. Acesso em: 12 mar. 2018.
Os estudos de ensaio clínico podem ser divididos em dois momentos:
A fase não clínica compreende o teste de medicamento e vacinas em laboratórios com animais de experimentação. Tem como objetivo principal verificar o funcionamento do produto em um organismo vivo. Para que os testes com os animais ocorram, é necessário que os pesquisadores sigam rigorosamente as normas de proteção aos animais de experimentação.
A fase clínica é a fase caracterizada pelos testes em seres humanos. Compreende quatro fases sucessivas, e somente após a conclusão de todas as fases é que o medicamento ou vacina poderá ser liberado para comercialização.
As fases são:
Um estudo de fase I testa o medicamento pela primeira vez; é a primeira avaliação de um produto químico ou biológico em seres humanos. O objetivo principal é avaliar a segurança do produto investigado, ou seja, avaliar toxicidade e farmacocinética do produto. Essa fase deve ser realizada no país em que a droga ou vacina foi produzida. É necessária uma supervisão médica constante e rigorosa. Normalmente é realizada em hospitais e o número de participantes da pesquisa nessa fase é limitado (média entre 10-30 voluntários, adultos sadios e geralmente do sexo masculino).
Caso o resultado dessa fase demonstre a segurança do produto, passa-se para a Fase II.
O objetivo dessa fase é avaliar a eficácia da medicação ou vacina, ou seja, a atividade terapêutica da droga ou atividade imunogênica da vacina, e obter informações mais detalhadas sobre a toxicidade do produto nos indivíduos para os quais o produto está sendo desenvolvido. Essa fase permite avaliar se o novo produto tem um efeito terapêutico, sendo definida a dose e a frequência de administração.
O número de participantes da pesquisa nessa fase é maior, normalmente de 70-100 voluntários, que são selecionados por meio de critérios rigorosos. O grupo é formado por uma população relativamente homogênea.
Caso o resultado dessa fase seja favorável, passa-se para a Fase III.
Nesta fase, o novo tratamento é comparado com o tratamento-padrão existente. É a fase do ensaio clínico, onde há a comparação entre os grupos. É utilizado um grande número de pacientes, normalmente entre 100 a 1000. Os voluntários são divididos em dois grupos:
Os grupos são randomizados, ou seja, a divisão entre os grupos é feita sob a forma de um sorteio. Os integrantes de cada grupo são escolhidos de forma aleatória. Os pacientes que entram em estudos na fase III têm chances iguais de cair em um ou outro grupo de estudo.
Algumas vezes, essa parte do estudo inclui vários grupos de pacientes tratados em serviços distintos (multicêntricos), mas sempre utilizando o mesmo protocolo de investigação.
A Food and Drug Administration (FDA ou USFDA) é a agência federal do Departamento de Saúde e Serviços Humanos dos Estados Unidos, órgão análogo a ANVISA nos Estados Unidos. Conheça mais acessando o link: <https://www.fda.gov/>. Acesso em: 12 mar. 2018.
Existem estudos que estudam a combinação de dois medicamentos, a fim de verificar o melhor resultado entre eles. Por exemplo, se a combinação do antibiótico X (novo) com o antibiótico Y (tratamento atual) é melhor do que o antibiótico Y para tratar uma determinada infecção.
Caso o resultado desta seja favorável, passa-se para a Fase IV.
Nesta fase, o medicamento já foi aprovado, registrado e está apto para comercialização. O objetivo dessa fase é acompanhar os efeitos dos medicamentos a longo prazo, estudar os riscos e os benefícios do medicamento, avaliar a dose-resposta, e detectar as reações adversas que são desconhecidas ou inadequadamente quantificadas em um maior número de doentes do que em fases anteriores do desenvolvimento clínico.
Os ensaios clínicos são estudos com um ótimo padrão de qualidade, mas apresentam alguns pontos desfavoráveis.
As principais desvantagens desse tipo de estudo incluem:
No Brasil, todos os ensaios clínicos com a participação de pessoas brasileiras, em todas as áreas da saúde, e com testes de todas as formas de intervenções, devem ser registrados no “Registro Brasileiro de Ensaio Clínico”. O coordenador, patrocinador do estudo ou um representante adequado, pode ser responsável pelo registro de um estudo, que deve ser feito após a aprovação de um comitê de ética nacional e antes do recrutamento do primeiro paciente.
Conheça mais sobre Registro Brasileiro de Ensaio Clínico. Acesse:
<https://ensaiosclinicos.gov.br/>. Acesso em: 12 mar. 2018.
Nas pesquisas de ensaio clínico, a randomização é um passo importante no delineamento do estudo. Nos estudos mais simples, um grupo de pessoas recebe o tratamento ativo e o outro grupo recebe o tratamento placebo. A alocação aleatória dos indivíduos nos dois grupos permite que fatores como idade, sexos e outras características sejam distribuídas de forma semelhante entre os grupos randomizados, estabelecendo a base para o teste da significância estatística das diferenças entre os grupos nos desfechos medidos.
Ao realizar o processo de randomização, o melhor cenário para a pesquisa é que cada grupo tenha o número igual de participantes. Em estudos com três ou mais grupos de comparação, a alocação dos indivíduos pode ser desigual, sendo que um dos grupos funcionará como controle para os demais.
Os procedimentos especiais de técnicas de randomização são:
Os procedimentos especiais de técnicas de randomização são:
Figura 3.3 – Randomização de pacientes.
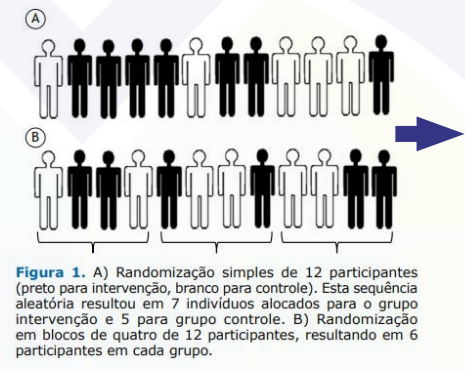
Fonte: Ferreira e Patino (2016).
Nessa aula, aprendemos as principais características das pesquisas de ensaio clínico. Entendemos a importância do ensaio clínico ao pontuar uma boa evidência sobre a área em questão, sendo ferramenta essencial para a tomada das melhores decisões na prática da Medicina Baseada em Evidências. Os estudos de ensaio clínico devem passar pela etapa não clínica e pelas quatro etapas clínicas. As novas terapias só podem ser colocadas no mercado após sua aprovação em todas as etapas de estudo clínico. Também aprendemos a importância do processo de randomização e suas diferentes técnicas.
A Diabetes Melito Gestacional é uma doença que exige um bom controle do índice glicêmico.
Leia o artigo disponível no link a seguir e responda as questões:
“Glibenclamida no Tratamento do Diabete Melito Gestacional em Estudo Comparado à Insulina”. Disponível em <http://bit.ly/u127bh>. Acesso em: 12 mar. 2018.
Analise o uso da metodologia de ensaio clínico para responder ao objetivo do estudo.
Os resultados encontrados nessa pesquisa auxiliam de que maneira no processo de tomada de decisão do profissional de saúde?
Qual a técnica de randomização utilizado no estudo?
Ressalta-se que o estudo de caso é uma ferramenta utilizada para aprofundar seus conhecimentos, não sendo considerada uma atividade avaliativa. Desta forma, não é necessário o envio de nenhum material relacionado ao estudo de caso aos canais de comunicação da Must University.
Referências Bibliográficas
Hulley, S.B., Cummings, S.R., Browner, W.S., Grady, D., Hearst, N. & Newman, T.B. (2015). Delineando a pesquisa clínica. Artmed. 4°ed.
Ferreira, J.C. & Patino, C.M. (2016). Randomização: mais do que o lançamento de uma moeda. J Bras Pneumol. n. 42, v.5, p310-10.

Livro de referência:
Hospital and Healthcare Security
by Tony W. York and Don MacAlister
Butterworth-Heinemann © 2015